炎症,是机体对刺激做出的一种防御反应,在生物体内起着重要的作用。当受到刺激因子(如病毒、细菌、机械损伤、强酸强碱等)的刺激时,会诱发炎症反应,从而修复受损组织,抵抗损伤。此外,炎症也会对机体产生不良影响,导致免疫系统紊乱。
近年来,有越来越多的研究报道了炎症与疾病的相关性,比如癌症、心血管疾病等。而在神经退行性疾病方面,炎症也起着重要作用,但具体的分子机制,哪些基因参与炎症调控影响疾病的发生发展,却是未知的。
在神经退行性疾病中,人们经常能观察到中枢神经免疫激活的现象。β干扰素,一类免疫调节因子,在抗病毒和抗炎症反应中起到至关重要的作用。研究者发现,缺少IFN-β,会促发一系列机制导致神经退行性疾病。
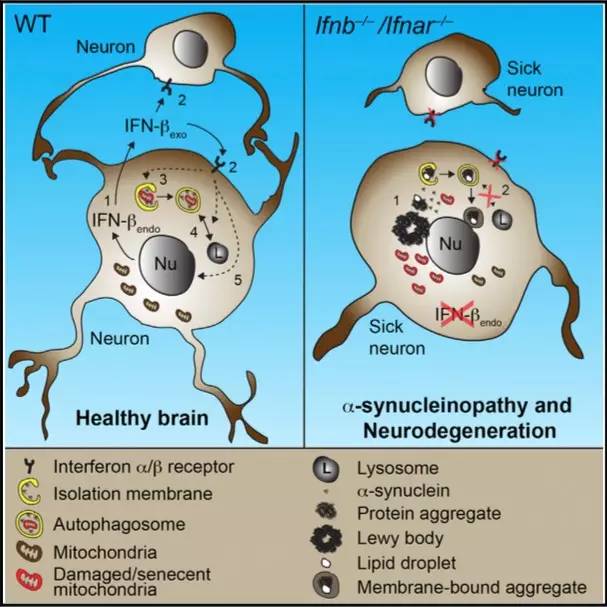
现象
机制
验证
研究人员敲除了小鼠ifnb基因,ifnb-/-小鼠随着年龄的增长,行动能力、抓力和学习能力出现明显的退化。海马组织中神经元的凋亡率上升以及数目下降。此外,神经元的树突变少变短,黑质纹状体区域酪氨酸羟化酶(Th)活性下降,同时伴随着多巴胺含量的减少。
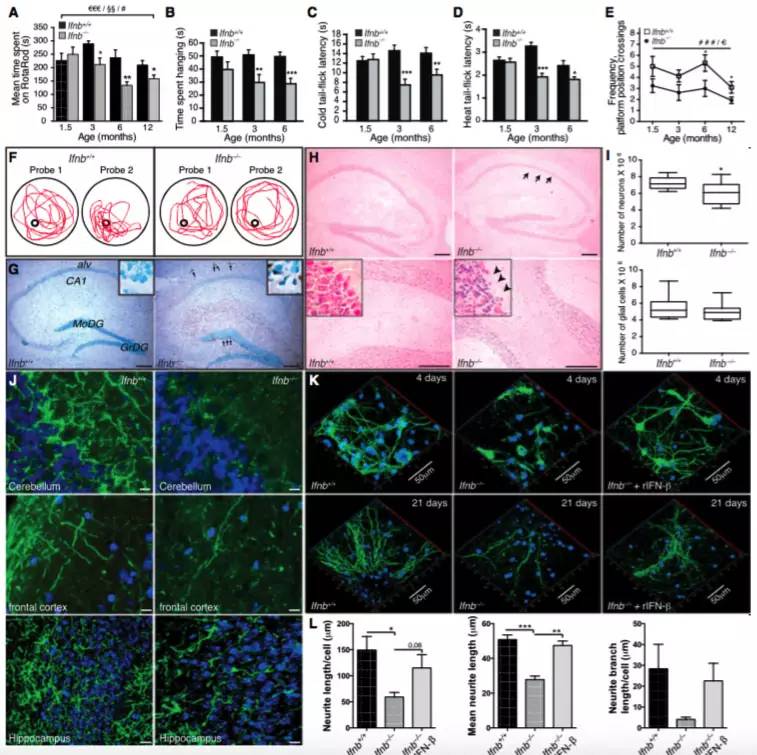
而帕金森病(PD)的主要特点是海马黑质区多巴胺含量减少,会影响抑制性乙酰胆碱的作用,从而导致震颤麻痹。而Ifnb-/-小鼠的种种表型与帕金森病类似。(ps:该种小鼠可以作为帕金森病样老年痴呆的动物模型,用以研究帕金森病的发病机制以及治疗方法。)
现象
机制
验证
科研工作者探索了Ifnb-/-小鼠出现帕金森病老年痴呆病症状的调控机制。通过大规模的全基因组测序,IFN-β信号通路和HD、PD、AD以及朊病毒疾病信号通路相关。

研究发现,Ifnb的缺失,会导致海马区α-synuclein 的积累,促进Lewy小体的形成,同时也会影响到自噬。在自噬阻断剂及注射α-synuclein表达质粒实验中,发现自噬阻断后可以引起α-synuclein的积累,而α-synuclein表达质粒却不会影响到自噬。因此Ifnb的缺失会影响自噬,促进α-synuclein的积累。
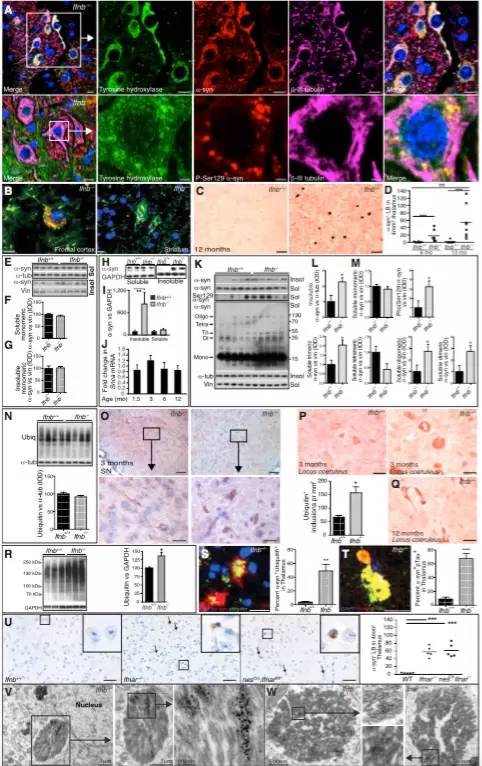
现象
机制
验证
为验证以上机制,科研工作者进行了回补实验:在Ifnb-/-小鼠中注射了IFN-β表达质粒,发现Ifnb-/-小鼠中各种异常表达的指标恢复了正常或者有所缓和,表明IFN-β的确可以调控自噬,影响α-synuclein的积累。
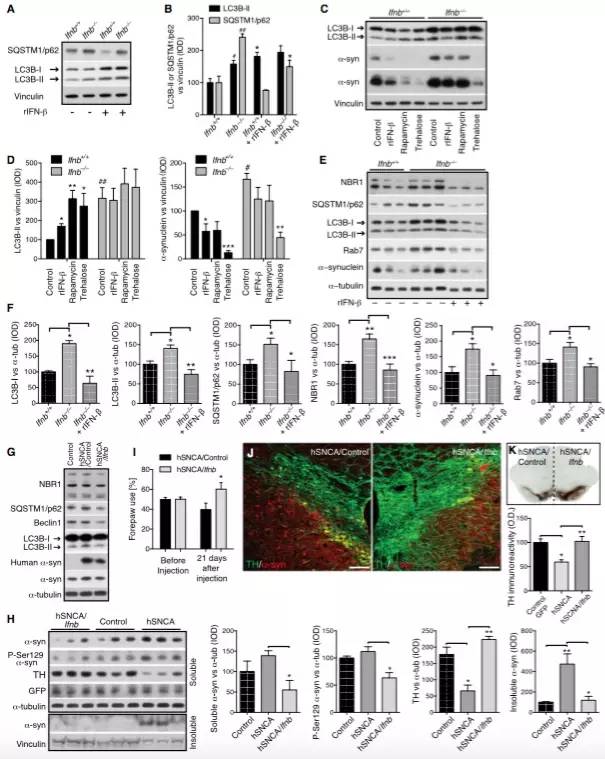
该研究遵循着“基于现有研究—提出假设—表型研究—机制探索—机制验证”的研究思路,运用基因敲除手段、质粒构建技术以及常规实验技术,融合了换物法、错位法、筛选法(科研创新的六脉神剑),研究证实了IFN-β在神经退行性疾病中起到了重要作用,为神经退行性疾病的发病机制研究和治疗研究提供了新的方向,拓宽了对此疾病的认知。
2016-05-27