毕赤酵母(Pichia pastoris) 是单细胞真核生物,它既具有原核生物易于培养、繁殖快和便于基因工程操作等特性, 同时又具有真核生物对基因产物正确折叠及翻译后加工及修饰能力, 所以毕赤酵母常用于表达外源蛋白。
影响毕赤酵母高效表达重组蛋白的因素很多,本文主要从分子水平上对影响因素进行总结分析,其中包括基因拷贝数、密码子偏爱性、启动子、分子伴侣、信号肽和糖基化修饰等因素, 并对发酵工艺进行概述。
1 基因拷贝数
基因拷贝数是毕赤酵母表达重组蛋白的一个影响因素。在一定范围内增加毕赤酵母中外源基因的拷贝数有利于重组蛋白的表达。但有时过高的外源基因拷贝数也会造成代谢负荷增加, 进而对宿主细胞产生负面影响, 使细胞活力下降。此外, 表达的目的基因不同,对于基因拷贝数的最佳选择也不相同。因此, 在进行实验设计时要对转入不同拷贝数基因的菌株进行比较, 才能确定最佳外源基因拷贝数。含高拷贝外源基因工程菌株的构建有不同的方法。
2 密码子偏爱性
密码子偏爱性是影响基因表达的重要因素。对于同义密码子而言, 不同物种的使用频率有很大差别,因此出现了所谓的密码子偏爱性。外源基因尤其是来自较远物种的基因在宿主中的表达会受到一定的影响, 通过对外源基因的密码子进行优化可以提高其表达水平。那些在同一物种中被频繁利用的密码子称为该物种的偏爱密码子; 不被经常利用的密码子称为稀有密码子。进行基因合成时一般使用偏爱密码子并避免使用稀有密码子, 基因的这种重新设计被称为密码子优化。通过选用毕赤酵母偏爱密码子和对基因GC 含量进行调整, 毕赤酵母中的重组蛋白表达量均可能得到有效提高。
3 启动子
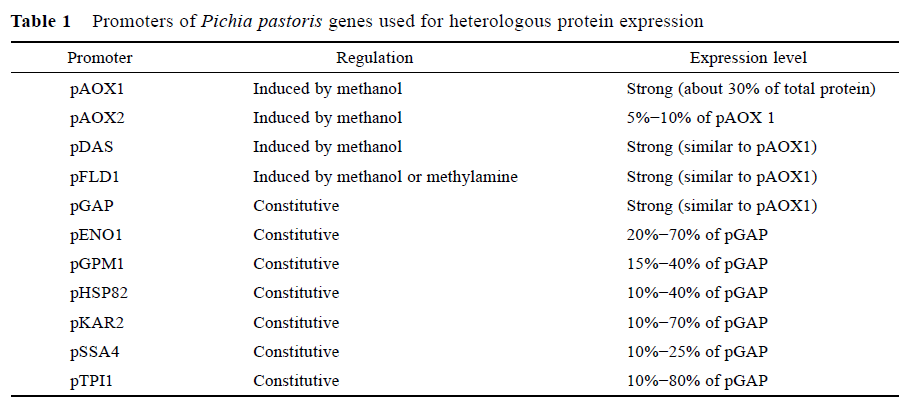
醇氧化酶基因启动子(pAOX) 是毕赤酵母表达外源蛋白最常用的启动子。pAOX 作为强启动子, 可以通过改变碳源严格控制外源基因的表达, 因此适合于表达毒性或有害的外源蛋白。在pAOX 控制下有些外源蛋白在毕赤酵母中表达量很大, 最高水平可达15 g?L?1 。但其也有不足之处, 毕赤酵母在不受抑制的条件下细胞先生长至高密度, 然后通过甲醇诱导启动外源蛋白表达, 这增加了工程菌的培养时间和工作量。同时在大规模生产过程中, 甲醇的使用也存在诸多弊端, 如易挥发、浓度不易检测、有潜在的火灾隐患、具有毒性、不适于药品和食品蛋白的生产等。正是由于pAOX 存在上述缺点, 人们开始研究其他启动子。尽管pAOX 和pGAP 作为强启动子可使外源基因在毕赤酵母中有很强的表达水平, 但有时也不利于外源蛋白的生产, 因为过量表达有时会导致蛋白折叠与定位错误, 此时较弱启动子更为可取。在选择启动子时, 必须依据研究目的和外源蛋白的性质来选择最合适的启动子, 有时并不是启动子越强越好, 合理选择与设计启动子是提高外源蛋白产量的有效途径。表1 为毕赤酵母常用的启动子。
4 分子伴侣
分子伴侣是一类在序列上没有相关性但有共同功能的蛋白, 其功能是在细胞内帮助其他蛋白完成正确的组装但不参与这些蛋白所行使的功能, 在组装完成后即与之分离。毕赤酵母分泌途径的限速步骤包括蛋白从内质网运输到到高尔基体, 其中内质网主要负责蛋白二硫键形成和蛋白折叠, 分子伴侣参与蛋白折叠过程。在内质网上的新生肽还可以通过与分子伴侣相互作用来维持其可溶形式。内质网上的分子伴侣主要包括蛋白质二硫键异构酶(proteindisulfide isomerase, PDI)、人免疫球蛋白结合蛋白(human immunoglobulin binding protein, BIP)、钙网蛋白和钙联接蛋白。其中的PDI 是硫氧化还原蛋白超家族之一, 它是催化二硫键形成和帮助蛋白正确折叠的多功能蛋白; BIP 主要通过结合到疏水性氨基酸延伸端来稳定未成熟的蛋白。由于分子伴侣在蛋白折叠中起着重要作用, 内质网上的分子伴侣通过操纵转录因子的水平, 改善毕赤酵母的蛋白分泌。大量研究报道, 分子伴侣与靶基因共表达可显著提高靶蛋白的表达量。
5 信号肽
在毕赤酵母中重组蛋白分泌到胞外必须经过信号肽的引导。由于信号肽与目的蛋白融合表达, 从而使目的蛋白在加工折叠后被引导分泌到胞外。常用的酵母信号肽有α交配因子信号肽(MF-α)、酸性磷酸脂酶信号肽(PHO1)、蔗糖酶信号肽(SUCZ)、Killer毒素信号肽和菊粉酶信号肽(INU) 等。MF-α是毕赤酵母表达重组蛋白时应用最广泛的一种信号肽,最常用的分泌型表达载体pPIC9K 和pPICZα-A 的信号肽就是MF-α。MF-α对引导小分子多肽和蛋白的分泌非常有效, 但对于引导大分子蛋白的分泌效果并不明显。近些年, 许多研究表明分泌信号肽是影响外源蛋白在毕赤酵母中表达的重要因素。
6 糖基化修饰
糖基化修饰是最重要的一种蛋白翻译后修饰。糖基化在参与免疫防御、受精、病毒复制、寄生虫感染、细胞生长和炎症等过程中起着重要作用。在真核生物中, 糖基化过程中加入的糖种类有显著差异。哺乳动物O-连接的寡糖主要是唾液酸、半乳糖和N-乙酰半乳糖胺, 毕赤酵母O-连接寡糖只是甘露糖残基。由于毕赤酵母特异性高度甘露糖基化的存在, 通常会使重组药物因为缺乏唾液酸糖基而被从血液中快速清除。也有研究证明, 通过对外源蛋白的糖基化位点进行改造, 可以提高外源蛋白在毕赤酵母中的表达。
7 发酵工艺
高密度发酵是提高毕赤酵母重组蛋白表达量的一种重要策略。毕赤酵母表达外源蛋白时, 温度、pH、碳源、溶氧等培养条件对目的蛋白的完整性及产量都有较大的影响, 优化培养条件可有效提高外源蛋白的表达量。对培养基的优化主要包括碳源的优化、氮源的优化、基础盐和PTM1 微量盐的优化。大量研究证明, 甲醇浓度对目的蛋白的表达起着重要作用。总之, 通过调节一种或综合调节多种发酵条件可显著提高重组蛋白的表达水平。
毕赤酵母作为一种表达外源基因的宿主菌, 既具有操作简单、生长速度快等特点, 又具有真核细胞的翻译后修饰加工系统, 且对营养要求低, 可采用廉价的培养基, 并适合于高密度发酵, 因此被广泛应用于重组蛋白表达, 成为最具吸引力的重组蛋白生产平台。但不同蛋白表达水平存在很大差异, 为提高外源蛋白的产量及活性, 需要对基因拷贝数、密码子偏爱性、启动子、分子伴侣、信号肽、糖基化修饰和发酵工艺等各方面因素综合考虑进行优化。然而, 毕赤酵母表达系统也存在一些不足, 如高密度发酵偏离细胞的天然生长条件。此外, 当蛋白过表达时, 许多蛋白产物对宿主细胞的生长存在严重的影响, 从而影响蛋白的表达量。因此, 通过分子伴侣提高蛋白折叠和分泌已经成为一个趋势。另一趋势是糖基化工程毕赤酵母与人源化重组糖蛋白的糖基化模式相结合,替代哺乳动物细胞表达系统, 从而减少生产时间和成本, 成为生产临床治疗用蛋白和其他蛋白的常用表达系统。
Souce: 纽普生物 2016-07-12