肥胖症在全球范围内影响超过5亿人,同时可能会导致2型糖尿病、心血管疾病以及癌症等疾病。FTO基因是一种与肥胖相关的等位基因,也称肥胖基因,由英国牛津大学马克·麦卡锡等研究人员首先鉴别出来,并发表在2007年4月的《科学》杂志上。FTO基因自发现以来一直是研究热点,涉及到FTO基因的文章在Pubmed上已经见刊就就达1695篇之巨,其中影响因子超过15的就达到76篇。
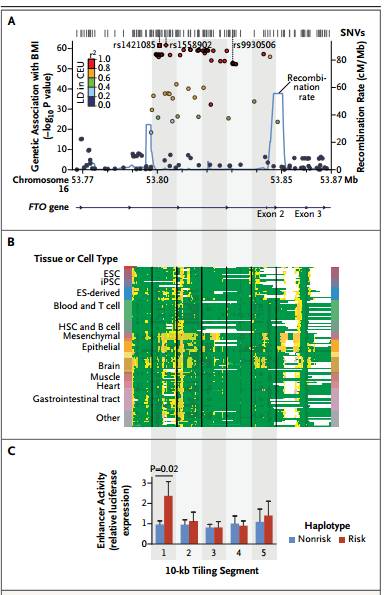
1. 全基因组关联研究(Genome-Wide Association Studies, GWAS)是一种利用全基因组SNP(Single-nucleotide polymorphism)分型技术,通过在全基因组水平上筛查与疾病或者是性状相关联的SNP,利用连锁不平衡来确定目标区域。其数据的处理是具有极大的挑战性的。肥胖与FTO等位基因中单核苷酸突变(SNV)rs1558902和rs1421085 具有极大的相关性。前者已经报导过。
2. 数据结果提示FTO等位基因与肥胖症相关联,以组织自制的方式通过抑制脂肪前体细胞线粒体产热。Rs1421085单点突变(T-C)导致模体结构改变成为ARID5B抑制者,在脂肪细胞分化的早期过程中其可以去除前脂肪细胞增强的抑制作用并使IRX3和IRX5的表达增加一倍。
3. 数据结果提示FTO等位基因与肥胖症相关联,以组织自制的方式通过抑制脂肪前体细胞线粒体产热。Rs1421085单点突变(T-C)导致模体结构改变成为ARID5B抑制者,在脂肪细胞分化的早期过程中其可以去除前脂肪细胞增强的抑制作用并使IRX3和IRX5的表达增加一倍。
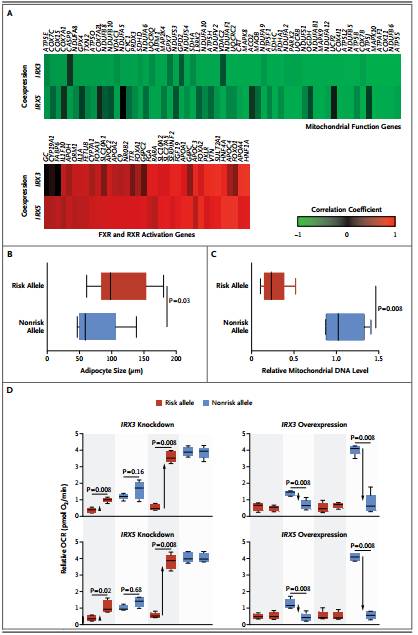
4. 这一过程导致的结果是使得耗能脂肪向储能脂肪进行转变,线粒体的产能作用降低了5倍,同时增加了脂肪储存的空间。抑制Irx3可以减轻小鼠的体重以及脂肪组织,同时在不改变食欲和运动量的情况下增加能量的消耗。
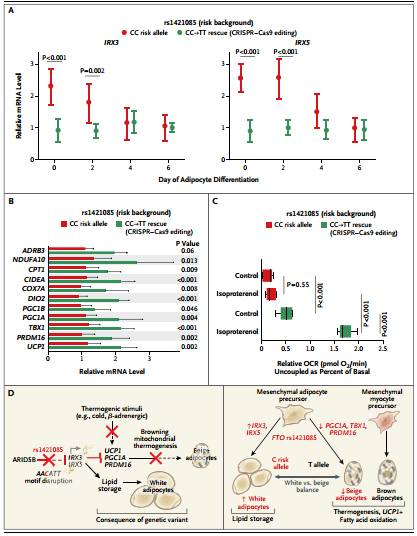
敲除参与者脂肪细胞中的IRX3和IRX5基因可以修复等位基因风险者的产能作用(增加了7倍),增加这些基因的表达则产生了相反的影响。
★. 本研究涉及表观基因遗传学,比较基因组学,人类遗传学,CRISPR基因编辑技术,通过小鼠模型,和人类标本,系统的研究了FTO单碱基突变和肥胖的联系和作用机制。结果表明脂肪细胞产热途径包括ARID5B,rs1421085,IRX3以及IRX5,分别对肥胖症有促进或抑制的作用。结果发表于医学四大刊物的《新英格兰医学杂志》。
该杂志以发表大量珍贵的临床研究资料。近年来基础和临床交互研究渐成热门,该杂志发表的基础性研究具有很高的临床应用价值。★
来源:百替生物
2016-06-02