对于非专业人士来说,血液是这样的。
去了医院抽血化验后,印象中的血就成了这样。

这还仅仅是一个普通的血常规,若真的想了解健康状况,一个住院病人的入院检查能抽十几个管子血,每一管子都能出一到两张这样的报告。
尤其是当碰到了癌症,现在血液中能检测到很多肿瘤标志物来进行参考。比如CEA和CA19-9增高多提示消化道肿瘤,但是这些标志物往往比较容易受影响,波动性很大,不具有很好的灵敏性和特异性。而近期大热的liquid biopsy不同于常规的标志物,它所检测的对象,是上述那些检测从未涉及的地方。癌症病人血液中会存在少量游离的循环肿瘤细胞(CTC)且坏死的癌细胞亦会释放少量的循环肿瘤DNA(ctDNA)到血液中,因此可通过检测从肿瘤原发或转移部位释放到血液中的CTC和ctDNA来检测癌症,即液体活检(Liquid Biopsy)。该技术被《MIT Technology Review》评为2015十大突破技术之一。那这CTC和ctDNA到底是什么东西呢?
CTC——流窜的罪犯
由于肿瘤细胞的无序繁殖需要掠夺大量的营养,而只在一地肯定无法满足这需求,因此就会发生肿瘤的转移和扩散。随着实体肿瘤的生长,在周围微环境发生了特定的变化时,就会促使一部分肿瘤细胞获得异常的活动能力。这些细胞从原发肿瘤上脱落,在身体里寻找新的落脚点。它们会通过血液系统或淋巴系统去往身体各处,搭乘血液快线的脱落肿瘤细胞就被称为循环肿瘤细胞(CTC)。当到达适宜的环境后,就会继续无限的繁殖,这就是肿瘤的血行转移,从原发部位形成继发性肿瘤。
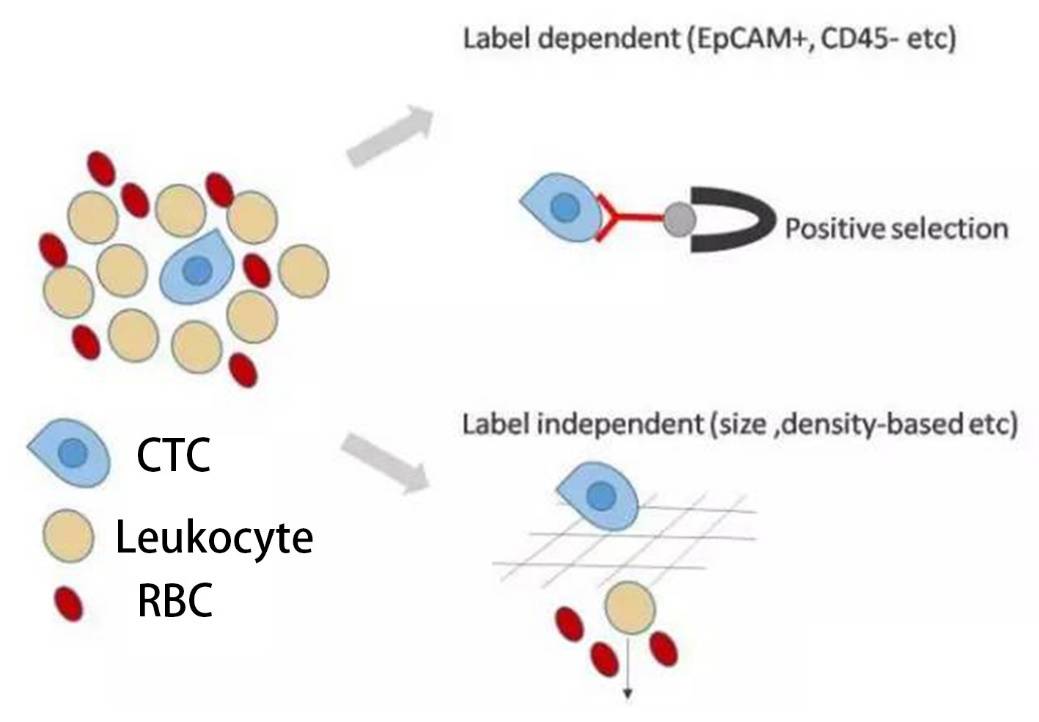
但在血液中要寻找CTC非常困难,因为每毫升血液里只有个位数的CTC,相比之下白细胞的数量是十万到百万级。红细胞就更多了,这要找起CTC来无异于大海捞针。不过如今有两件工具来帮助我们寻找CTC:筛子和钩子。
正如上图所示,CTC的大小和白细胞的大小有着细微的差别,因此我们可以用特定的筛子去筛选出体积较大的CTC。但是筛子的滤网只认体积,所以个子小的肿瘤细胞有可能漏下去,让我们误以为没有CTC细胞的检出,造成假阴性结果;个子大些的或者聚成团的白细胞,则可能无法穿过滤网,造成假阳性。另一种方法,就是用钩子。钩子是根据CTC专门设计的,通过抗原抗体的识别功能,对CTC表面有而普通血细胞没有的抗原分子,进行特异性的吸附。基于这种原理,我们可以分离收集到绝大多数的CTC,大大提高了灵敏度和特异性。
虽然影像学检测能看出实体肿瘤的大小,但与肿瘤的恶性程度和转移情况不一定成正比。而CTC能反应肿瘤的转移程度,这些脱落的细胞本就是实体瘤的一部分,得到他们就相当于取得了实体瘤的组织,可以对肿瘤进行多种检测,以便了解病情,优化治疗方案。
ctDNA——特殊标记
ctDNA和蛋白类标记物相比,前者的检测更灵敏,很少出现假阳性,可跟踪肿瘤的消失、扩散和复发。因为它是DNA,所以它是自带信息的物质,一般是来源于凋亡裂解的细胞。而肿瘤细胞破裂释放到血液中的游离DNA,就是ctDNA。
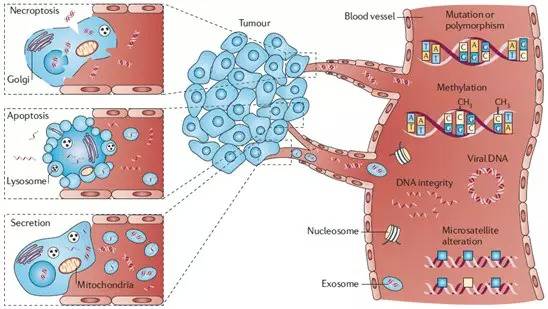
Liquid Biopsy检测通过测定ctDNA可以实现癌症分型和检测治疗产生的耐药情况,为癌症复发提供早期预警,为药物治疗时产生耐药提供依据。之前我们提到血液里面的肿瘤细胞分离都不容易,我们更没办法把这些DNA分离出来了。得益于测序成本的下降,和大规模平行测序技术的发展,我们不必在分子层面去分离ctDNA,而是通过测序,利用肿瘤细胞基因组的特点,从携带信息的层面去挑出属于肿瘤细胞的部分。并且由于ctDNA可来自于任何裂解的肿瘤细胞,更能反映出肿瘤细胞整体的基因变异信息。
对于ctDNA深度分析有助于发现新的耐药基因。测序技术的进步为血液检测的引领奠定了基础。外周血ctDNA外显子组测序加快了第三代EGFR TKI耐药机制的研究。
Liquid Biopsy检测能有助于实现基因检测从单一基因到多基因,静态到动态,定性到定量,有创到无创的境界,是推动精准医疗基础上个体化治疗的领航者。Liquid Biopsy目前具有高的特异性和好的疗效预测性,并能较好地克服肿瘤组织的异质性,故可作为组织检测的补充或替代。在《Clinical Cancer Advance 2015》报告中,液体活检技术也被列为今后十年内可广泛应用的一项癌症检测技术。
来源:解螺旋
2016-06-06