手性碳原子是指与四个各不相同原子或基团相连的碳原子,用C*表示。判断手性碳原子的方法:确认碳原子是饱和的; 碳原子所连接的四个基团必须各不相同。
自然界中大约有500多种氨基酸,但是从最小的生物到我们人类,所有物种中的蛋白质主要由20种氨基酸组成,而这些氨基酸均为α-氨基酸。α-氨基酸可用通式RCH(NH2)COOH表示。甘氨酸的R=H,所以除了甘氨酸之外,α-氨基酸中的α碳原子都是手性碳原子。α-氨基酸中的碳原子可以用R/S构型标记,但是研究早期这些氨基酸均有了相应的俗名,我们就更习惯用D/L构型法标记。
D/L构型是将分子经过费歇尔投影(Fischer projection)处理后得到的平面结构与甘油醛的构型比较而确定的。费歇尔投影式是表示单糖链形结构、氨基酸等有机化合物结构的一种常用方法。
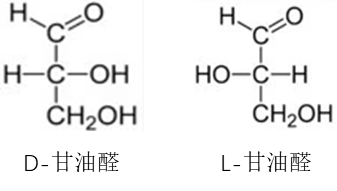
Fig 1. D/L甘油醛
以丙氨酸为例:
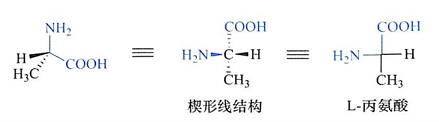
Fig 2. L-丙氨酸的费歇尔投影
羧基写在竖线上方,R基写在竖线下方,氨基和氢写在横线两侧。若氨基的位置L-甘油醛中的羟基位置一致,就定义为L-氨基酸;反之,则定义为D-氨基酸。对氨基酸来说,横线两侧与α碳原子相连的两个原子伸出纸面朝向我们的眼睛,竖线方向的两个原子指向纸内远离我们的眼睛。
R-S构型标记法适用于具有手性碳原子(点手性)、手性轴(轴手性)的分子结构,手性碳原子可造成两种不同的立体构型——R构型(rectus)和S构型(sinister),该两种构型的定义为:将与手性碳原子相连的四个基团按顺序规则排列大小,最小的基团放在离眼睛最远的地方,其他三个基团按由大到小的方向旋转,若旋转方向是顺时针,则手性碳为R构型;若为逆时针,则手性碳为S构型。
对于R/S 构型的判断,根据手性碳原子(与四个各不相同的原子或基团相连的碳原子)周围的四个不同基团的排列顺序来确定的。
例如,对于手性碳连接的四个基团分别为 —H、—OH、—CH3、—NH2,比较这四个基团中直接与手性碳相连的原子,即 H、O、C、N 的原子序数。原子序数大小顺序为 S>O>N>C>H,所以 —OH 优先于 —NH2,—NH2优先于 —CH3,—CH3优先于 —H。随后通过右手螺旋法,将最小的基团(也就是H)设置在远离观察者的位置,其他三个基团对着观察者。如果三个基团顺时针旋转,则为R构型,反之为S构型。
以丙氨酸为例:
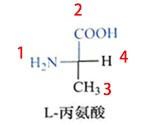
Fig 3. L-丙氨酸的Cahn–Ingold–Prelog (CIP)顺序规则
H原子原子序数最小,编号为4;对于20种自然氨基酸来说,氨基上的N原子序数最大,所以编号为1;羧基和甲基与α碳相连的都是C原子,排不出顺序,就继续考察与这些C相连的最大原子,羧基上C连接的最大原子是O,甲基上C连接的最大原子是H,所以O>H,所以羧基编号为2,甲基编号为3;从1到3的顺序是顺时针(如果此时α碳连接的H原子是远离我们的,则为R型),但是α碳连接的H原子是指向我们的,所以旋转顺序需要反向,就变成了逆时针,就是S型。
按照类似的规则,我们可以发现L-Cys是R型,而其他L-型氨基酸都是S型。
因此20种自然氨基酸中,除了甘氨酸外,有19种氨基酸的α碳都是手性原子,他们存在L/D型之分。除了L-Cys是R型外,其他的18种L型氨基酸都是S型;相反地,除了D-Cys是S型外,其他的18种D型氨基酸都是R型。
Souce: 纽普生物 2024-09-05